非电解质的含义是什么
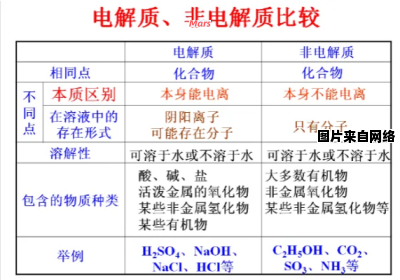
不是电解质与非电解质的区别?
电解质 是指可以产生自由离子而导电的化合物。通常指在溶液中导电的物质,但熔融态及固态下导电的电解质也存在。电解质通常分为强电解质和弱电解质。 强电解质 指的能完全或基本完全电离成为离子的 化合物 。 通常包含三类物质: 强酸:如硫酸、硝酸、盐酸等 强碱:如氢氧化钠、氢氧化钾 大多数的盐:如氯化钠、氯化钾 注意:是否是强电解质与溶解度无关。如硫酸钡,虽为难溶物,但其溶于水的部分完全电离了,所以将其划分为强电解质。
电解质与非电解质知识点总结?
当我们研究溶液的性质时,电解质和非电解质是两个重要的概念。它们描述了溶质在溶液中的行为和电导性质。以下是电解质和非电解质的知识点总结:
**电解质:**
1. **定义:** 电解质是在水或其他溶剂中能够离解成离子的物质。这意味着电解质在溶液中能够导电,因为溶液中存在自由移动的离子。
2. **分类:** 电解质可以分为强电解质和弱电解质。
- **强电解质:** 在溶液中几乎完全离解成离子,导电性能非常好。例如,强酸(如盐酸)、强碱(如氢氧化钠)。
- **弱电解质:** 在溶液中只部分离解成离子,导电性能相对较差。例如,弱酸(如乙酸)、弱碱(如氨水)。
3. **离子化:** 电解质在溶液中通过离子化过程将分子转化为离子,其中正离子称为阳离子,负离子称为阴离子。
4. **例子:** 盐、酸、碱等都属于电解质,它们在水中能够产生离子,从而使溶液具有导电性。
**非电解质:**
1. **定义:** 非电解质是指在溶液中无法离解成离子的物质。这意味着非电解质在溶液中不能导电,因为溶液中没有可移动的离子。
2. **特点:** 非电解质分子在溶液中保持原来的分子状态,不发生离解。
3. **例子:** 葡萄
什么是电解质什么是非电解质?
电解质是一种在极性溶剂(如水)中溶解时产生导电溶液的物质
非电解质是以典型的共价键结合的化合物,它们在水溶液中不发生电离反应。除羧酸及其盐、酚、胺以外,大多数有机化合物都是非电解质,如 蔗糖、甘油、 乙醇等。在无机化合物中,只有某些非金属的 卤化物和所有非金属氧化物(除了水)是非电解质

非电解质有哪些类型?
常见的非电解质包括:蔗糖、甘油、乙醇、一氧化碳、二氧化碳、甲烷、氨气等。
非电解质是以典型的共价键结合的化合物,它们在水溶液中不发生电离反应。除羧酸及其盐、酚、胺以外,大多数有机化合物都是非电解质。在无机化合物中,只有某些非金属的卤化物和所有非金属氧化物(除水)是非电解质。
具体可以分为:
1、非金属氧化物:一氧化碳、二氧化碳、二氧化硫、五氧化二磷。
2、很多有机物:乙烷、四氯化碳、乙醇、乙醛、酯、蔗糖。
3、部分氢化物:甲烷、硫化氢。
常见的非电解质有:非金属氧化物,CO、CO2、SO2、P2O5;很多有机物,乙烷、四氯化碳、C2H5OH、乙醛、酯、蔗糖;部分氢化物,CH4、NH3(H2O、H2S、HCl是电解质)。非电解质是指在水溶液里和熔融状态下都不能导电的化合物。
上一篇:小米如何与萧艾的同学建立联系
下一篇:华为如何应对小窗口通知的挑战?
