极性键与非极性键的不同之处是什么?
极性键和非极性键的区别?
记给你最好的教育
在学习化学这门学科的时候,会接触到非极性键和极性键,不过有些朋友容易将非极性键和极性键混淆,这两者只要按照相应标准区分,还是很好区别的,那么非极性键和极性键的区别是什么呢?
非极性键和极性键的区别包含了以下罗列的几个方面:
1、含义不同,分子中,同种原子形成的共价键就是非极性键。化合物分子中,不同种的原子形成的共价键就是极性键。
2、主要特点不同。非极性键共用电子对不偏向任何一个原子。极性键主要特点是共用电子对向氧化性强的粒子偏移。
3、成键原子显电性状况不同,不显电性的形成了非极性键,显电性的形成了极性键。
极性键=
在化合物分子中,不同种原子形成的共价键,由于两个原子吸引电子的能力不同,共用电子对必然偏向吸引电子能力较强的原子一方,因而吸引电子能力较弱的原子一方相对的显正电性。这样的共价键叫做极性共价键,简称极性键。
举例:hcl分子中的h-cl键属于极性键
判别
同种原子之间的是非极性键

极性键存在于不同种元素间
但是存在极性键的物质不一定是极性分子.
区分极性分子和非极性分子的方法:
非极性分子的判据:中心原子化合价法和受力分析法
1、中心原子化合价法:
组成为abn型化合物,若中心原子a的化合价等于族的序数,则该化合物为非极性分子.如:ch4,ccl4,so3,pcl5
2、受力分析法:
若已知键角(或空间结构),可进行受力分析,合力为0者为非极性分子.如:co2,c2h4,bf3

3、同种原子组成的双原子分子都是非极性分子。
不是非极性分子的就是极性分子了
常见极性分子:
hx,co,no,h2o,h2s,no2,so2,scl2,nh3,h2o2,ch3cl,ch2cl2,chcl3,ch3ch2oh
非极性键=
由同种元素的原子间形成的共价键,叫做非极性键。同种原子吸引共用电子对的能力相等,成键电子云对称地分布在两核之间,不偏向任何一个原子,成键的原子都不显电性。非极性键可存在于单质分子中(如h2中h—h键、o2中o=o键、n2中n≡n键),也可以存在于化合物分子中(如c2h2中的c—c键)。非极性键的键偶极矩为0。以非极性键结合形成的分子都是非极性分子。存在于非极性分子中的键并非都是非极性键,如果一个多原子分子在空间结构上的正电荷几何中心和负电荷几何中心重合,那么即使它由极性键组成,那么它也是非极性分子。由非极性键结合形成的晶体可以是原子晶体,也可以是混合型晶体或分子晶体。例如,碳单质有三类同素异形体:依靠c—c非极性键可以形成正四面体骨架型金刚石(原子晶体)、层型石墨(混合型晶体),也可以形成球型碳分子富勒烯c60(分子晶体)。
怎样区别极性键和非极性键?
区别在于它们的电子云的分布方式。
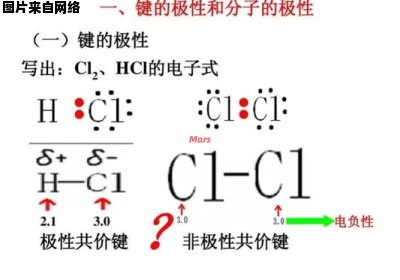
极性键:当化学键形成时,原子的电子云会被吸引到一个原子的某一侧,使得这一侧的电荷分布变得更密集,而另一侧的电荷分布则变得较稀疏。这种化学键就被称为极性键。在极性键中,原子中心存在一个极性,在化学反应中,这个极性可能会影响化学反应的速率、方向和产物的选择等。
非极性键:当两个原子之间形成的化学键时,原子的电子云相互重叠,电子云的分布均匀,两端不存在电荷分布不均匀的现象,因此这种化学键被称作非极性键。在非极性键中,原子中心不存在极性,它们在化学反应中的作用相对较小。
总之,区分极性键和非极性键,要观察化学键两端的原子的电子云的分布情况,如果存在电荷分布不均匀的情况,则是极性键。反之,则是非极性键。
极性键和非极性键怎么区别?
1、含义不同,分子中,同种原子形成的共价键就是非极性键。化合物分子中,不同种的原子形成的共价键就是极性键。
2、主要特点不同。非极性键共用电子对不偏向任何一个原子。极性键主要特点是共用电子对向氧化性强的粒子偏移。
3、成键原子显电性状况不同,不显电性的形成了非极性键,显电性的形成了极性键。
上一篇:如何做到言行一致,成为真正的君子
下一篇:脚汗引起的原因及应对方法
