石墨与金刚石的特性差异有何不同之处?
金刚石与石墨不同为什么?
1、晶体结构不同
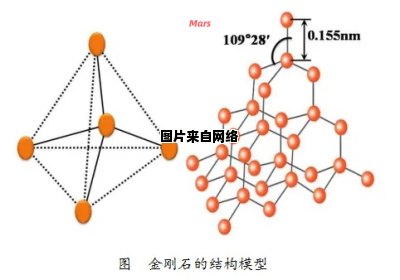
石墨是正六边形的晶体结构,并且它属于分子晶体。金刚石则是正八边形的结构,它属于原子晶体,相互之间是正正四面体的。石墨会有鳞片一样的质感但是很细腻而且有滑腻的感觉。
2、外观颜色不同
石墨一般是深灰色的,它的表面会散发着像金属一样的光泽。金刚石则是颜色更多,它有无色的,也有半透明的,还有全透明的,也有黑色的,但其中无色的是最好的,半透明的次之,黑色的较差。
3、物理化学特性不同
石墨的硬度要低于金刚石,后者被称为自然界里面存在的最坚硬的误会,所以石墨是相对质地较软的。但是在化学特性上,石墨的熔点要比金刚石膏,所以它更耐热和耐高温以及腐蚀。
从组织的角度分析石墨和金刚石的异同?
相同之处是组成石墨和金刚石的都是碳。不同的是分子的排列不同。组成金刚石的分子是接立体正三角形排列。而石墨分子之间是平面排列的。由于分子排列的不同而呈现出不同的物理性质。如金刚石透明且质地坚硬。而石墨则呈黑色且质地柔软等。
金刚石和石墨都有什么区别?
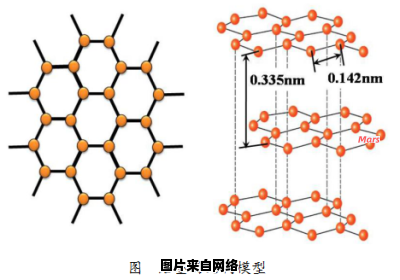
石墨是层状结构,碳原子是sp2杂化,形成正六边形,每个层状结构就是这个六边形构成,层与层之间是范德法力,作用比较弱,然后碳原子还有一个电子空余,形成一个很大的π键,因此导电性、导热性很好.金刚石是共价晶体,碳原子是sp3杂化,形成正四面体结构,很稳定,因为碳原子由八个电子然后都是电子对,共价晶体
根本区别是共价键的数量不同, 金刚石是全共价键的,形成了立体的框架结构, 石墨是非全共价键的,想成了平面的层状结构。 这样金刚石和石墨虽然是完全相同的元素组成的, 但是物理性质差异巨大,金刚石硬度极大,石墨缺很软。 希望对你有帮助。
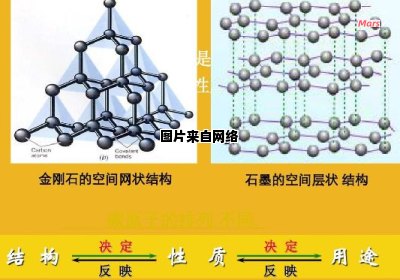
金刚石和石墨都是由碳组成的,但它们的物理性质又有天壤之别,金刚石是碳原子在高温高压下以正方体结构形成的,纯净的金刚石通体透明且硬度是自然界已知最硬的物体,而石墨是碳原子以片状结构构成的,颜色为黑色,质地较软有导电性。以上就是金刚石和石墨的区别。
上一篇:相宜本草红景天适合哪种肤质?
下一篇:实用的呼叫转移设置方法
