勒夏特列原理研究温度的影响
为什么越稀越电离?从勒夏特列来解释?
溶液越稀时,会通过电离生成更多的离子来减弱对溶液的稀释。
根据勒夏特列原理可知,在一个已经达到平衡的反应中,如果改变影响平衡的条件之一(如温度、压强,以及参加反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动。
所以说当溶液越来越稀时,溶液中粒子的浓度降低(水自身浓度不变),所以化学平衡向减弱粒子浓度减小的方向移动,换言之就是生成更多的离子来减少这种变化,因此促进了弱酸或弱碱的电离。
扩展资料
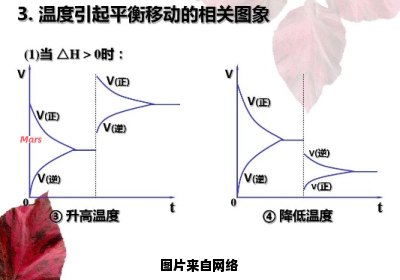
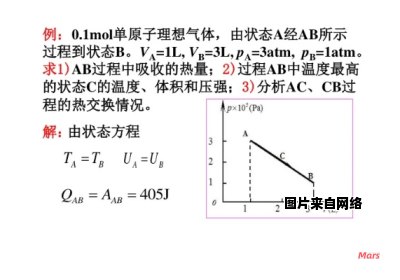
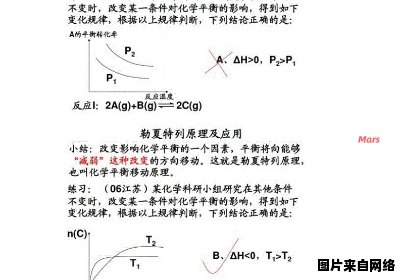
勒夏特列原理是涉及平衡问题中最重要的一个原理,几乎所有的平衡移动的问题都可以用勒夏特列原理来解释和判断,包括浓度、压力、温度的改变对化学反应的影响。
1、浓度改变
增加某一反应物的浓度,则反应向着减少此反应物浓度的方向进行,即反应平衡向正反应方向移动进行。减少某一生成物的浓度,则反应向着增加此生成物浓度的方向进行,即反应平衡向正反应方向移动进行。反应速率及产率也会因为对外界因素系统的影响而改变。
2、温度改变
升高反应温度,则反应向着减少热量的方向进行,即放热反应逆向进行,吸热反应正向进行;降低温度,则反应向着生成热量的方向的进行,即放热反应正向进行,吸热反应逆向进行。
3、压力改变
压力同样仍是朝消除改变平衡因素的方向进行反应。增加某一气态反应物的压强,则反应向着减少此反应物压强的方向进行,即反应向正方向进行。减少某一气态生成物的压强,则反应向着增加此生成物压强的方向进行,即反应向正方向进行。反之亦然。
上一篇:用成语形容中秋的习俗
下一篇:玉溪市公积金管理中心负责人
